黄斑病变(专业版)
黄斑是视网膜的一部分,它负责中心视觉。视网膜是眼睛后部的组织,它向大脑发送视觉信号。黄斑变性是老年人黄斑破坏的最常见原因,它会逐渐失去敏锐的中心视觉。
英文名称:Adult Macular Degeneration;Age-Related Macular Degeneration, AMD
定义
黄斑是视网膜的一部分,它负责中心视觉。视网膜是眼睛后部的组织,它向大脑发送视觉信号。黄斑变性是老年人黄斑破坏的最常见原因,它会逐渐失去敏锐的中心视觉。这种疾病属于衰老性疾病,但在少数情况下,可能发生在年轻人身上。成人或年龄相关性黄斑变性(AMD),被归类为:
- 早期:中型玻璃膜疣显示存在早期的AMD。玻璃膜疣是黄色沉积物在视网膜上发现的,但是,视力仍不受影响。
- 中期:大型玻璃膜疣的出现,有或者无在视网膜色素的变化。视力减退可能发生,但多数人没有症状。
- 晚期:随着玻璃膜疣发展,视力和黄斑损害出现。晚期AMD可以是:
- 干性黄斑变性,或称萎缩性AMD:当视网膜的某一部位病变时,这种情况就会发生。这导致黄斑细胞的缓慢分解,中心视野逐渐丧失。干性AMD约占85%。
- 湿性黄斑变性,或称渗性AMD:随着干性AMD恶化,新血管可能开始形成。这些新血管常在黄斑下渗出血液和液体。这会导致黄斑区永久性损害。湿性AMD并不常见,但它是导致失明的主要原因。
病因
AMD的原因尚不很清楚,一般认为基因、光积聚损伤、自由基损伤和血液动力学因素等综合作用。可能包括如下机制:- 氧化应激:视网膜尤其易受到氧化应激引起的损伤,因为它耗氧量大、需要高比例的不饱和脂肪酸以及曝露于可见光。这些区域存在高浓度的维生素C以吸收光辐射。
- 炎症:视网膜上皮细胞炎症和损伤,引起营养物代谢障碍,进一步导致视网膜损伤。
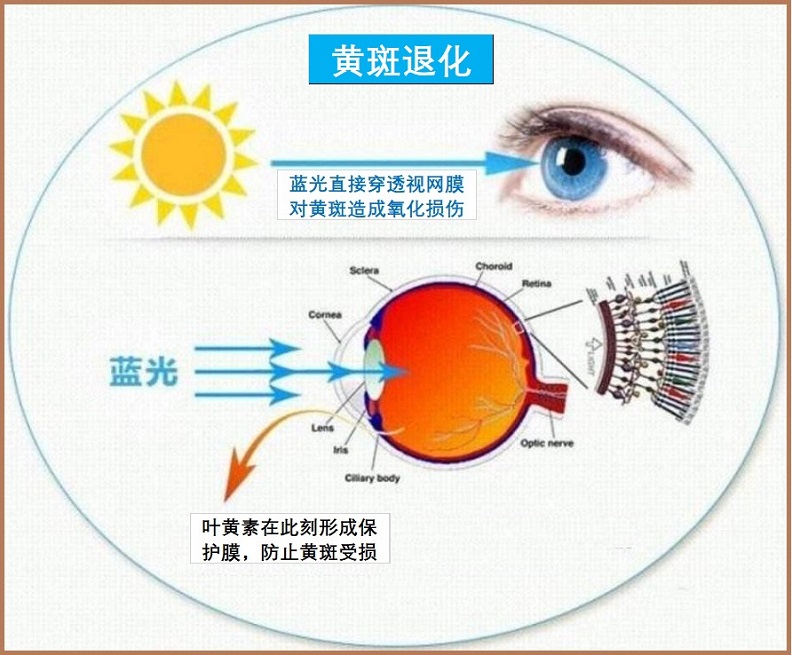
- 光毒性:暴露于蓝色和紫外(UV)辐射,对视网膜产生不利影响。
- 营养不良或缺失:类胡萝卜素类(如叶黄素、玉米黄质等)和B族维生素摄入不足等。
- 一些健康状况也引起视网膜变性,如糖尿病、高血压等。
风险因素
AMD的风险随着年龄的增长而增加,在老年女性中更常见。其他可能增加AMD的风险因素包括:
- 吸烟,或二手烟
- 饮酒过量
- 家庭成员患AMD
- 过度暴露于阳光下
- 心血管病,如高血压或高胆固醇
- 饮食营养不良,如缺乏绿叶菜类等
症状
在一些人中,AMD进展缓慢,对视力没有明显影响。而在另一些患者中,这种疾病发展得更快,并可能导致显著的视力丧失。症状可能包括如下:
- 视力模糊
- 看到细节困难,比如看书认字等
- 视力模糊,在明亮的光下
- 小的,但越来越多的盲点在视野中
- 直线(如门框)出现弯曲或扭曲
疗法
治疗取决于AMD的分期阶段。综合疗法可包括如下:
调整饮食与生活方式
- 健康均衡饮食,富含果蔬菜,尤其是绿叶菜类。
- 经常食用豆制品,有助于防止湿性AMD。
- 深海鱼类、亚麻籽油和坚果等。
- 不抽烟或戒烟,吸烟对AMD发生和发展密切相关。
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控黄斑病变的营养和草本补充剂,主要包括如下:
1.黄斑色素与叶黄素等:
黄斑色素(MP)密度与AMD发病之间的关系已得到很好的证实。MP主要由三种类胡萝卜素组成:叶黄素、玉米黄质和消旋玉米黄质(Meso-Zeaxanthin)。它们分别约占视网膜类胡萝卜素总含量的36%、18%和18%。它们存在于黄斑和周围组织中,包括滋养视网膜的血管和毛细血管1。
叶黄素、玉米黄质和消旋玉米黄质通过过滤有害的紫外线并充当抗氧化剂来确保黄斑的正常功能2,3。在衰老过程中,叶黄素和玉米黄质的水平下降;低水平的MP与AMD有关4。一项对捐赠眼睛的尸检研究发现,与对照组相比,黄斑变性患者的三种类胡萝卜素水平都降低了。然而,最重要的发现是黄斑变性受试者黄斑中的消旋玉米黄质急剧减少5。这项尸检研究有助于证实其他研究,这些研究表明所有三种类胡萝卜素在维持黄斑结构完整性方面的重要性6。这些类胡萝卜素通过其抗氧化特性和滤光能力保护黄斑和下方的感光细胞7。
摄入叶黄素和玉米黄质是一项重要的预防措施,但也可能逆转正在进行的退化过程8。由于叶黄素和玉米黄质具有所有类胡萝卜素的组织特异性特征,它们的自然倾向是集中在黄斑和视网膜中。摄入富含这些物质的食物尤其重要,因为它们对黄斑色素密度有直接影响—色素密度越大,发生视网膜撕裂或变性的可能性就越小9。黄色或橙色的水果(例如芒果、奇异果、橙子以及深绿叶、橙色和黄色品种的蔬菜)是叶黄素和玉米黄质的来源5。
与叶黄素和玉米黄质不同,饮食中不含有消旋玉米黄质,但需要它维持年轻的黄斑密度10。与健康眼睛的人相比,黄斑变性患者黄斑中的消旋玉米黄质减少了30%。当作为补充剂服用时,消旋玉米黄质被吸收到血流中,并有效提高黄斑色素水平10。
2.花青素和C3G:
C3G(花青素-3-葡糖苷)是越橘的关键成分,也是强大的抗氧化剂11,12。在许多动物研究和一些人类研究中,使用越橘治疗黄斑变性以及其他眼部疾病,包括糖尿病视网膜病变、色素性视网膜炎、青光眼和白内障,已经注意到了积极的结果13,14。C3G已被证明可以通过使人眼中负责夜视的杆状细胞更快地恢复功能来改善人类的夜视能力15。在动物细胞中,C3G再生视紫红质(吸收光的视网膜复合体)11。越橘中的花青素通过与血管胶原相互作用降低血管通透性,从而减缓酶对血管壁的攻击。这可以防止在新生血管AMD中普遍存在的毛细血管渗漏。研究还表明越橘增加了眼睛的氧化应激防御机制14。添加维生素E可能会带来额外的好处16。
C3G具有高度的生物可利用性,可增强身体的其他功能17-19。其强大的抗氧化特性保护组织免受DNA损伤,这通常是癌症形成和组织衰老的第一步20,21。
C3G保护内皮细胞免受过氧亚硝酸盐诱导的内皮功能障碍和血管衰竭的影响22。此外,C3G通过抑制诱导型一氧化氮合酶(iNOS)来对抗血管炎症23。同时,C3G上调内皮一氧化氮合酶(eNOS)的活性,有助于维持正常的血管功能24。这些对血管的影响在视网膜中尤为重要,视网膜中脆弱的神经细胞依赖于单一的眼动脉来维持。
在动物模型中,C3G可以预防肥胖并改善血糖升高25。其中一种方法是增加有益的脂肪相关细胞因子脂联素的基因表达26。当然,糖尿病患者容易出现严重的眼部问题,包括血糖水平升高导致失明。
最后,人们发现C3G在脑功能的实验细胞模型中具有神经保护作用,有助于防止阿尔茨海默症相关蛋白淀粉样蛋白β对脑细胞的负面影响27。
3.藏红花:
藏红花(或番红花)通常用于烹饪香料,尤其作为在地中海和中东地区的原产地。它也可以用作草药,并含有几种类胡萝卜素,包括番红花苷(Crocin)、番红花酸(Crocetin)和番红花醛(Safranal)28,29。临床前研究发现,藏红花及其成分促进健康的视网膜血流,并有助于保护视网膜细胞免受光照和氧化应激引起的损伤29-32。
多项临床试验表明,藏红花可能是治疗AMD的可行药物。在一项随机、对照、交叉试验中,25名早期AMD受试者在三个月内每天服用20mg藏红花或安慰剂,然后转入替代干预。视网膜闪烁敏感性是黄斑健康的标志,使用藏红花而不是安慰剂可以改善33。研究人员随后评估了长期益处:当29名早期AMD受试者平均服用相同剂量的藏红花14个月时,视网膜灵敏度不仅提高了3个月,而且视力也提高了,与基线相比,受试者能够在标准视力测试图上平均多读两行。在长达15个月的随访期内保持了改善34。在另一项针对早期AMD患者的研究中,在平均每天服用20mg藏红花11个月后,无论参与者是否有遗传易感性,视网膜敏感性都会提高35。
在另一项专门考虑干性AMD的研究中,每天50mg藏红花,持续三个月,显著改善了视力和对比敏感度,而对照组没有明显改善36。在一项针对100名轻度至中度AMD患者的更大规模交叉研究中,与安慰剂相比,连续三个月每天服用20mg藏红花显著提高了视觉准确性和视网膜反应速度37。藏红花在临床和临床前研究中也被证明有助于预防其他常见的眼部疾病38-40。
4.银杏叶:
银杏叶可以改善眼睛的微血管循环,减缓黄斑的恶化41。银杏叶通过抑制血小板聚集和调节血管弹性,改善主要血管和毛细血管的血液流动。银杏也是一种强大的抗氧化剂42。
5.葡萄籽提取物:
葡萄籽提取物是一种生物类黄酮,是一种强效抗氧化剂。植物衍生的生物类黄酮在食用时很容易被人体吸收。生物类黄酮似乎可以保护视网膜神经节细胞43。对果蝇进行的研究表明,葡萄籽提取物可以减弱病理蛋白的聚集,这表明它对黄斑变性和神经退行性疾病有保护作用。因此,施用葡萄籽提取物的果蝇表现出改善的眼睛健康44。在糖尿病动物身上进行的类似实验表明,葡萄籽提取物限制了糖尿病视网膜病变(视网膜退化)中出现的眼血管损伤,这与AMD有一些共同的病理特征45。
令人信服的实验室证据表明,葡萄提取物可以抑制人体细胞中的血管生成46。这表明葡萄籽提取物可以抑制在湿性AMD中观察到的异常血管生长。
6.维生素C和谷胱甘肽:
作为抗氧化剂,谷胱甘肽和维生素C在健康的眼睛中含量很高,在AMD患者的眼睛中数量减少。维生素C有助于眼睛合成谷胱甘肽。当与半胱氨酸(一种氨基酸抗氧化剂)结合时,半胱氨酸在水溶液中保持稳定,是谷胱甘肽合成的前体。维生素C很重要,因为它能吸收紫外线辐射,而紫外线辐射会导致白内障47。局部维生素C抑制炎症性新生血管形成动物模型中的新生血管形成48。
7.肌肽(滴眼液):
L-肌肽是一种天然存在的抗氧化剂和抗糖化剂。研究表明肌肽可抑制脂质过氧化和自由基诱导的细胞损伤49。局部应用N-乙酰基半乳糖苷可以防止光诱导的DNA链断裂,修复受损的DNA链50,并改善患有晚期白内障的动物和人类的视力、眩光和晶状体混浊51,52。
8.硒:
硒是一种必需的微量矿物质,是抗氧化酶谷胱甘肽过氧化物酶的一种成分,对减缓AMD和其他眼部疾病(包括白内障和青光眼)的进展很重要53,54。在小鼠中,谷胱甘肽过氧化物酶表达的增加可保护其免受氧化诱导的视网膜变性的影响55。
9.辅酶Q10:
辅酶Q10是一种重要的抗氧化剂,可以保护眼睛免受自由基损伤56。线粒体DNA(mtDNA)不稳定性是线粒体损伤的一个重要因素,最终导致与年龄相关的变化和病理。在眼睛的所有区域,mtDNA损伤都会因衰老和年龄相关疾病而增加57。在一项研究中,抗氧化剂的组合,包括辅酶Q10、乙酰L肉碱和ω-3脂肪酸,改善了视网膜色素上皮线粒体的功能,随后稳定了早期AMD患者的视觉功能58。
10.牛磺酸和硫辛酸:
牛磺酸是一种在视网膜中高浓度存在的氨基酸。牛磺酸缺乏会改变视网膜的结构和功能59。硫辛酸被认为是一种“通用抗氧化剂”,因为它是脂肪和水溶性的。它还可以减少小鼠的脉络膜新生血管形成60。因此,二者均可预防AMD发生发展。
11.维生素B族:
维生素B2(核黄素)可减少氧化型谷胱甘肽,有助于防止光敏感性、视力丧失以及眼睛灼热和瘙痒61。
AMD病因的最新进展揭示了心血管疾病(CVD)的共同风险因素以及类似的潜在机制,特别是炎症和CVD的生物标志物升高,包括C反应蛋白(CRP)和同型半胱氨酸62。研究人员发现,同型半胱氨酸水平升高和某些B族维生素水平低(对同型半胱氨酸代谢至关重要)与老年人患AMD和视力下降的风险增加有关63。
一项强有力的研究发现,补充叶酸、维生素B6和维生素B12可以显著降低有心血管危险因素的成年人患AMD的风险64。这些数据,再加上其他的验证性研究,说服了医生建议AMD患者补充维生素B。一项针对5000多名女性的研究表明,在饮食中加入叶酸(2.5mg/天)、B6(50mg/天,)和B12(1mg/天)可以预防和降低AMD的风险64。
12. 关于年龄相关眼病研究的营养素(AREDS和AREDS2)
AMD营养补充剂的最大和最重要的研究是年龄相关眼病研究(AREDS和AREDS2)65,66。
- 第一次AREDS证明,当每天给患有晚期湿性和干性AMD的人服用β-胡萝卜素(7500mcg RAE/15 mg)、维生素C(500mg)、维生素E(180mg/400IU)、锌(80mg)和铜(2mg)时,进展为终末期AMD的风险降低。数千名患者接受了长达6年的随访。AREDS显示AMD患者有显著改善,因此对大多数AMD患者提出了广泛的配方建议,但双眼晚期患者除外67。
- 由于对补充β-胡萝卜素存在争议,即在当前和以前的吸烟者中观察到肺癌风险增加。因此,进行了AREDS2以评估更新配方的疗效。在AREDS2中,用叶黄素(10mg)加玉米黄质(2mg)代替β-胡萝卜素。AREDS2试验还将一些参与者的锌剂量降至25 mg。对4000多名有发展为晚期AMD风险的参与者进行了平均五年的随访。研究人员得出结论,叶黄素加玉米黄质可能是β-胡萝卜素的合适类胡萝卜素替代品,尤其是对以前吸烟者来说,因为这种替代品与最初的AREDS配方相当。此外,较低剂量的锌不会影响疗效66。
建议了解更全面的相关营养素内容,可参阅本网站专文:眼健康 >>
更多可点击其个性化综合干预方案如下:
- 黄斑病变防控(改善早期症状)
- 黄斑病变防控(抑制黄斑退化)
- 黄斑病变防控(防止视力下降)
- 黄斑变性防控(50-60岁)
- 黄斑变性防控(61-70岁)
- 黄斑变性防控(71-80岁)
- 黄斑变性防控(81岁以上)
以及了解有关内容参阅本网如下专文:
医疗干预
常规治疗措施包括如下:
- 医生将定期检查AMD的任何变化或进展。
- 治疗主要是针对晚期黄斑病变(湿性)。因为这个阶段视力下降可能很严重。
预防
有助于减少AMD发生的措施,包括如下:- 按照医生建议,定期检查眼睛。
- 咨询医生应该如何补充维生素和矿物质等。
参考文献:
1. Rapp LM et al. Lutein and zeaxanthin concentrations in rod outer segment membranes from perifoveal and peripheral human retina. Invest Ophthalmol Vis Sci. 2000 Apr;41(5):1200-9.
2. Beatty S et al. The role of oxidative stress in the pathogenesis of age-related macular degeneration. Surv Ophthalmol. 2000 Sep-Oct;45(2):115-34.
3. Kaya S et al. Effect of lutein supplementation on macular pigment optical density in patients with AMD. Acta Ophthalmologica. 2010 Sep;88(s246).
4. Johnson EJ et al. Intake of lutein and zeaxanthin differ with age, sex, and ethnicity. J Am Diet Assoc. 2010 Sep;110(9):1357-62.
5. Bone RA et al. Lutein and zeaxanthin in the eyes, serum and diet of human subjects. Exp Eye Res. 2000 Sep;71(3):239-45.
6. Krinsky NI et al. Biologic mechanisms of the protective role of lutein and zeaxanthin in the eye. Annu Rev Nutr. 2003;23:171-201.
7. Landrum JT et al. Lutein, zeaxanthin, and the macular pigment. Arch Biochem Biophys 2001 Jan 1;385(1):28-40.
8. Richer S et al. Double-masked, placebo-controlled, randomized trial of lutein and antioxidant supplementation in the intervention of atrophic age-related macular degeneration: the Veterans LAST study (Lutein Antioxidant Supplementation Trial). Optometry. 2004 Apr;75(4):216-30.
9. Stahl W. Macular carotenoids: lutein and zeaxanthin. Dev Ophthalmol. 2005;38:70-88.
10. Bone RA et al. Macular pigment response to a supplement containing meso-zeaxanthin, lutein and zeaxanthin. Nutr Metab (Lond). 2007 May 11;4:12.
11. Amorini AM et al. Activity and mechanism of the antioxidant properties of cyanidin-3-O-beta-glucopyranoside. Free Radic Res. 2001 Dec;35(6):953-66.
12. Zafra-Stone S et al. Berry anthocyanins as novel antioxidants in human health and disease prevention. Molecular Nutrition & Food Research. 2007 Jun;51(6):675-683.
13. Fursova AZ et al. Dietary supplementation with bilberry extract prevent macular degeneration and cataracts in senesce-accelerated OXYS rats. Adv Gerontology. 2005;16:76-79.
14. Milbury PE et al. Bilberry (Vaccinium myrtillus) Anthocyanins modulate heme oxygenase-1 and glutathione S-transferase-pi expression in ARPE-19 cells. Invest. Ophthalmol. Vis. Sci. 2007 May;48(5):2343-2349.
15. Nakaishi H et al. Effects of black currant anthocyanoside intake on dark adaptation and VDT work-induced transient refractive alteration in healthy humans. Alt Med Rev. 2000 Dec;5(6):553-62.
16. Roberts LJ et al. The relationship between dose of Vitamin E and suppression of oxidative stress in humans. Free Radical Biology and Medicine. 2007 Nov;43(10):1388-1393.
17. Miyazawa T et al. Direct intestinal absorption of red fruit anthocyanins, cyanidin-3-glucoside and cyanidin-3,5-diglucoside, into rats and humans. J Agric Food Chem. 1999 Mar;47(3):1083-91.
18. Tsuda T et al. Absorption and metabolism of cyanidin 3-O-beta-D-glucoside in rats. FEBS Lett. 1999 Apr 23;449(2-3):179-82.
19. Matsumoto H et al. Orally administered delphinidin 3-rutinoside and cyanidin 3-rutinoside are directly absorbed in rats and humans and appear in the blood as the intact forms. J Agric Food Chem. 2001 Mar;49(3):1546-51.
20. Acquaviva R et al. Cyanidin and cyanidin 3-O-beta-D -glucoside as DNA cleavage protectors and antioxidants. Cell Biol Toxicol. 2003 Aug;19(4):243-52.
21. Riso P et al. Effects of blood orange juice intake on antioxidant bioavailability and on different markers related to oxidative stress. J Agric Food Chem. 2005 Feb 23;53(4):941-7.
22. Serraino I et al. Protective effects of cyanidin-3-O-glucoside from blackberry extract against peroxynitrite-induced endothelial dysfunction and vascular failure. Life Sci. 2003 Jul 18;73(9):1097-114.
23. Pergola C et al. Inhibition of nitric oxide biosynthesis by anthocyanin fraction of blackberry extract. Nitric Oxide. 2006 Aug;15(1):30-9.
24. Xu JW et al. Cyanidin-3-glucoside regulates phosphorylation of endothelial nitric oxide synthase. FEBS Lett. 2004 Sep 10;574(1-3):176-80.
25. Tsuda T et al. Dietary cyanidin 3-O-beta-D-glucoside-rich purple corn color prevents obesity and ameliorates hyperglycemia in mice. J Nutr. 2003 Jul;133(7):2125-30.
26. Tsuda T et al. Anthocyanin enhances adipocytokine secretion and adipocyte-specific gene expression in isolated rat adipocytes. Biochem Biophys Res Commun. 2004 Mar 26;316(1):149-57.
27. Tarozzi A et al. Neuro-protective effects of cyanidin 3-O-glucopyranoside on amyloid beta (25-35) oligomer-induced toxicity. Neurosci Lett. 2010 Apr 5;473(2):72-6.
28. Alavizadeh SH et al. Bioactivity assessment and toxicity of crocin: a comprehensive review. Food and chemical toxicology: an international journal published for the British Industrial Biological Research Association.Feb 2014;64:65-80.
29. Fernandez-Sanchez L et al. Natural Compounds from Saffron and Bear Bile Prevent Vision Loss and Retinal Degeneration. Molecules.2015;20(8):13875-13893.
30. Ahmadi N et al. Assessment of saffron neuroprotective properties in rat retina versus light damage. Research Journal of Pharmacognosy. 2020;7(2):33-42.
31. Chen L et al. Neuroprotective effects of crocin against oxidative stress induced by ischemia/reperfusion injury in rat retina. Ophthalmic research.2015;54(3):157-168.
32. Xuan B et al. Effects of crocin analogs on ocular blood flow and retinal function. Journal of ocular pharmacology and therapeutics: the official journal of the Association for Ocular Pharmacology and Therapeutics. Apr 1999;15(2):143-152.
33. Falsini B et al. Influence of saffron supplementation on retinal flicker sensitivity in early age-related macular degeneration. Investigative ophthalmology & visual science. Dec 2010;51(12):6118-6124.
34. Piccardi M et al. A longitudinal follow-up study of saffron supplementation in early age-related macular degeneration: sustained benefits to central retinal function. Evidence-based complementary and alternative medicine: eCAM.2012;2012:429124.
35. Marangoni D et al. Functional effect of Saffron supplementation and risk genotypes in early age-related macular degeneration: a preliminary report. Journal of translational medicine.2013;11:228.
36. Riazi A et al. The impact of saffron (Crocus sativus) supplementation on visual function in patients with dry age-related macular degeneration. Italian Journal of Medicine. 2017;11(2):196-201.
37. Broadhead GK et al. Saffron therapy for the treatment of mild/moderate age-related macular degeneration: a randomised clinical trial. Graefe's Archive for Clinical and Experimental Ophthalmology. 2019;257(1):31-40.
38. Jabbarpoor Bonyadi MH et al. The ocular hypotensive effect of saffron extract in primary open angle glaucoma: a pilot study. BMC complementary and alternative medicine. 2014;14:399.
39. Makri OE et al. Saffron administration prevents selenite-induced cataractogenesis. Molecular vision.2013;19:1188-1197.
40. Bahmani F et al. Inhibitory Effect of Crocin(s) on Lens alpha-Crystallin Glycation and Aggregation, Results in the Decrease of the Risk of Diabetic Cataract. Molecules.2016;21(2):143.
41. Thiagarajan G et al. Molecular and cellular assessment of Ginkgo biloba extract as a possible ophthalmic drug. Experimental Eye Research. 2002 Oct;75(4):4231-430.
42. Mahadevan S et al. Multifaceted therapeutic benefits of Ginkgo biloba L.: Chemistry, efficacy, safety and uses. Journal of Food Science. 2008 Jan/Feb;73(1):R14-R19.
43. Majumdar S et al. Potential of the bioflavonoids in the prevention/treatment of ocular disorders. Journal of Pharmacy and Pharmacology. 2010 Aug;62(8):951-965.
44. Pfleger CM et al. Grape-seed polyphenolic extract improves the eye phenotype in a Drosophila model of tauopathy. Int J Alzheimers Dis. 2010 Aug 24;2010. pii: 576357.
45. Li M et al. A novel approach of proteomics to study the mechanism of action of grape seed proanthocyanidin extracts on diabetic retinopathy in rats. Chin Med J (Engl). 2008 Dec 20;121(24):2544-52.
46. Liu M et al. Antiangiogenetic effects of 4 varieties of grapes in vitro. J Food Sci. 2010 Aug 1;75(6):T99-104.
47. Tan AG et al. Antioxidant nutrient intake and the long-term incidence of age-related cataract: the Blue Mountains Eye Study. Am J of Clin Nutr. 2008 Jun;87(6):1899-1905.
48. Peyman GA et al. Inhibition of corneal angiogenesis by ascorbic acid in the rat model. Graefes Arch Clin Exp Ophthalmol. 2007 Oct;245(10):1461-7.
49. Guiotto A et al. Carnosine and carnosine-related antioxidants: a review. Curr Med Chem. 2005;12(20):2293-315.
50. Specht S et al. Continuing damage to rat retinal DNA during darkness following light exposure. Photochem Photobiol. 2000 May;71(5):559-66.
51. Williams DL et al. The effect of topical antioxidant formulation including N-actetyl carnosine on canine cataract: a preliminary study. Vet Ophthalmol. 2006 Sep-Oct;9(5):311-6.
52. Babizhayez MA et al. N-acteylcarnosine sustained drug delivery eye drops to control the signs of ageless vision: Glare sensitivity, cataract amelioration and quality of vision currently available treatment for the challenging 50,000 patient population. Clin Interv Aging. 2009 May;4:31-50.
53. Head KA. Natural therapies for ocular disorders, part 2: cataracts and glaucoma. Altern Med Rev. 2001 Apr;6(2):141-66.
54. King AJ. Should we be considering selenium in glaucoma? Br J Ophthalmol. 2009;93(9):1132-1133. doi:10.1136/bjo.2008.141218.
55. Lu L et al. Increased expression of glutathione peroxidase 4 strongly protects retina from oxidative damage. Antioxidants & Redox Signaling. 2009 Apr;11(4): 715-724. doi:10.1089/ars.2008.2171.
56. Blasi MA et al. Does coenzyme Q10 play a role in opposing oxidative stress in patients with age-related macular degeneration? Ophthalmologica. 2001 Jan-Feb;215(1):51-4.
57. Jarrett SG et al. The importance of mitochondria in age-related and inherited eye disorders. Ophthalmic Res. 2010;44(3):179-90.
58. Feher J et al. Improvement of visual functions and fundus alterations in early age-related macular degeneration treated with a combination of acetyl-L-carnitine, n-3 fatty acids, and coenzyme Q10. Ophthalmologica. 2005 May-Jun;219(3):154-66.
59. Hussain AA et al. Taurine transport pathways in the outer retina in relation to aging and disease. Ocular Transporters in Ophthalmic Diseases and Drug Delivery. Ophthalmology Research 2008(V):217-233.
60. Dong A et al. Oxidative stress promotes ocular neovascularization. Jour of Cellular Physiol. 2009 Jun;219(3):544-552.
61. Lopez B et al. Artificial tear composition and promotion of recovery of the damaged corneal epithelium. Cornea. 1993 Mar;12(2):115-20.
62. Vine AK et al. Biomarkers of cardiovascular disease as risk factors for age-related macular degeneration. Ophthalmol. Dec 2005;112(12):2076-80.
63. Rochtchina E et al. Elevated serum homocysteine, low serum vitamin B12, folate, and age-related macular degeneration: The Blue Mountains Eye Study. Am J Ophthalmol. 2007 Feb;143(2):344-6.
64. Christen WG et al. Folic acid, vitamin B6 and vitamin B12 in combination with age-related macular degeneration in a randomized trial of women. Arch Intern Med. 2009 Feb 23;169(4):335-41.
65. AREDS Report number 8 (Age-Related Eye Disease Study). A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss. Arch Opththalmol 2001;119:1417-1436.
66. AREDS2 Research Group. Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013 May 15;309(19):2005-15.
67. Fahed DC et al. Impact of AREDS in a developing country 5 years after publication of the study. Eur J Ophthalmol. 2011 Jan-Feb;21(1):67-72.
68. Chew EY, Clemons TE, Agrón E, et al. Long-term Outcomes of Adding Lutein/Zeaxanthin and ω-3 Fatty Acids to the AREDS Supplements on Age-Related Macular Degeneration Progression: AREDS2 Report 28. JAMA Ophthalmol. J JAMA Ophthalmol. 2022 Jul 1;140(7):692-698.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国黄斑变性基金会
https://www.macular.org
美国眼视力网站
http://www.eyesight.org
加拿大黄斑变性国际联盟
http://www.amdalliance.org
加拿大验光协会
https://opto.ca
其他参考文献:详见具体的综合干预方案
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

